1) はじめに;
昭和30年代、豊倉がまだ大学院の学生の頃、当時の化学工学協会ではじめての総合
シンポジウムを開催された。その時藤田重文先生が「 困っている問題 」というセッションを設置しようと提案されたと伺った。その時先生は幾つかの話題を例に出されたが、その中に「結晶の成長と溶解」があって、城塚先生が早稲田大学で引き受けられ、研究室で晶析実験を行っていた豊倉が話題提供の準備をすることになった。
当時、東京工業大学の藤田研では 2004B-1,3で記述したように谷本先生が結晶の成長速度と溶解速度の差から結晶が成長している時の結晶表面における結晶成長速度係数を求めておられ、結晶の成長と溶解は文字の上からは可逆的な現象のように考えられていたが、藤田研ではこれらの現象は可逆的でないという考えを持っていたように推測した。 そこで、豊倉は、実験室で予備的な簡単なテストを行い、文献で勉強した結晶が成長する時の表面に存在している溶質と結晶の結びつき等を検討した。
2) 結晶の成長と溶解の予備的な検討:
2・1)過飽和溶液内で成長してる結晶表面に存在してる溶質と結晶の結びつき;
当時の文献の説明では、”過飽和溶液に置かれた大きな結晶表面上に小さな立方体溶質が存在すると、その溶質は立方体の1面の持っている力で結晶に引き寄せられ、その表面上を比較的自由に動くことは出来るが、大きな力がかからないと結晶表面から溶液内に離脱することはない。この溶質が結晶表面上を動いてステップの下の凹みに移動して来てそこに止まると、その溶質は結晶と2面の持ってる力で引き寄せられるのでこのステップに到着した溶質は結晶表面上の1面で引き寄せられてるものより安定である。更にこの溶質がステップに沿って移動し、そのステップが他の面と交叉しているキンクに到着するとそれは3面で結晶に引き寄せられるようになる。言い換えると、このキンクに引き寄せられた溶質は最も安定した状態で結晶に固定されることになる。” 過飽和溶液内の現象がこの単純化したモデルで表わせる場合を想定して考えた。そこで、溶液内の溶質が大結晶と衝突する可能性を考えるとその頻度はは過飽和濃度に比例する。また結晶表面上の溶質はその温度の飽和濃度に比例して結晶表面より溶液内に散逸して行くと考えるとその差の溶質量が結晶表面上存在することになる。 その内一部はキンクやステップに到着し、結晶に組み込まれる。またあるものは2次元核の発生となり、結晶表面上の新たなステップやキンクの生成となって結晶成長になる。さらに過飽和溶液中に非常に小さい結晶が発生していると、それは結晶に付着してあたかも2次元核が発生したと同じように結晶成長に寄与することがある。一方、結晶表面上のステップやキンクは溶質を取り込みながら移動し、その過程で消滅することもあるが、また溶質を取り込みなが移動をしても消滅することなく成長を続けるものもある。それらの個々の機構はすでにある程度研究されてるものもあったが、それらを総括的に検討し、装置内の結晶成長機構に基づく結晶成長速度の定量化に成功した報告はない。
2・2)結晶が溶解する時の溶質の結晶から溶液中への離脱;
僅かに未飽和な溶液中に存在する結晶表面上の溶質状態を考えると、立方体結晶表面に組み込まれた小さな立方体溶質の5面はそれぞくベースになっている結晶と強い力で引きあっている。それに対して溶液内に散逸しようとする力は溶液に接している1面のみに作用するので、その散逸はなかなか起こらない。それに対して、立方体結晶の稜や頂点に存在する立方体溶質は2面や3面が溶液に接しており、結晶表面上の他の溶質より結晶との結びつきは弱く散逸しやすいと考えられる。そのことは未飽和溶液の中に存在する立方体結晶の頂点に存在する結晶は1番溶解しやすく、次いで稜に存在する溶質が溶解すると考えられる。そこで、立方体結晶を考えて、その頂点にある立方体溶質が抜けたとするとその抜けた溶質結晶と3面で接していた立方体の稜にあった3ヶ所の立方体溶質は元の結晶の新しい頂点になる。そうすると、1頂点の立方体溶質が抜けると3倍の溶解しやすい立方体溶質が生まれることになる。このように結晶の溶解現象を結晶成長現象同様、結晶表面における立方体溶質の挙動として考えると結晶は溶解が進むと益々溶け易くなると考えられる。
2・3)未飽和溶液中の直方体結晶の溶解現象の観察;
実験室の塩素酸ナトリウムの晶析実験で生成した透明なNaClO3直方体結晶を静置未飽和塩素酸ナトリウム水溶液に入れて観察実験を行った。その時の結晶形状の変化は未飽和度の大きさによって異なるが、どの場合も結晶表面化から溶解が一様に進むのでなく、立方体結晶の頂点に近い稜の部分から浸食が始まり、時間の経過につれて、稜の結晶が欠けるように欠落し、それと同時に、遥かに微細な結晶も溶解しつつ結晶周辺に落下するのが確認された。このような欠落が進むのは、晶析段階で結晶が成長する時、溶質は結晶格子へ正しく配列して生成するのでなく、部分的に正しく配列をして生成したものが合一して比較的大きい結晶になっていて、未飽和溶液内では液がその結晶中に浸透することによって、結晶の溶解が進むためと考えた。また僅かに未飽和状態にした溶液を静かに流した中に結晶を入れるとその溶液が直接結晶に当たる平面の4辺の稜の部分の溶解が早く進んだが、その初期段階では、結晶の頂点の部分から微結晶が欠落するように溶解が進み、その結晶を取り出して観察すると溶解は進んだ部分の面は粗くなっていた。
2・4)予備的検討の総括;
結晶を未飽和溶液内で僅かに溶解させると、結晶の頂点や、稜の部分の溶解が優先的に進んで、頂点や稜の部分の形状は曖昧になった。そこでこの未飽和溶液を別に調整したの過飽和溶液に替えて流すと、稜線が曖昧であった結晶の頂点や稜の線が明瞭になり、その結晶は短時間の内に溶解実験開始前の形状に戻った。これらを2・1)~2・3)の検討と比較して総括すると、結晶の溶解現象も結晶の成長現象同様、溶液本体内と結晶表面に接している溶液との間に溶質の拡散現象があり、また結晶表面では成長・溶解両現象ともそれぞれに特有な表面現象が存在するであろうと考えて、次の溶解・成長実験を行って検討した。
3) 流動溶液中における固定単一塩素酸ナトリウム結晶の成長・溶解実験:
[ この研究は化学工学29巻、2号、122(1965)に掲載された ” 塩素酸ナトリウム結晶よりの結晶成長速度 ” の一部を使用〈晶析工学の進歩; p199 の記事参照〉 ]
この実験で使用した装置は2004B-2,2で紹介したU字形テスト装置で、操作法はその時の方法と殆ど同じですが、測定値はテスト前後に実測された塩素酸ナトリウム結晶重量とそのテスト時間です。結晶成長時の重量増加に対する相関式は広く使用されてる 式〈1〉を用いた。
1/M・dW/d |
=KoA(Cb-Cs)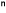 (1) (1) |
|
= KDA(CbーCI )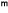 (2) (2) |
|
=KRA(CIーCs)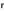 (3) (3) |
ここで、M, W,  , Ko, KD, KR, A, C はそれぞれ分子量、結晶質量、時間、総括結晶成長速度係数、拡散段階の物質移動係数、結晶表面段階の結晶成長速度係数、溶液濃度(添字b,s,I はそれぞれ溶液本体内、結晶表面温度に対応した飽和濃度、結晶表面の溶液濃度を示す)である。式(1)は結晶成長速度を総括値で表わしたものです。この現象はさらに溶質が溶液本体内より結晶表面へ拡散する段階と結晶表面に到着した溶質が、結晶格子に組み込まれる表面晶析段階に分けて考えられ、それらをそれぞれ式(2)、(3)で示した。この現象は直列機構で式(2)、(3)はそれぞれ式(1)と等しいと表示したが、速度的に考えるとその機構は全く異なりそれらは一般的には等しくない。しかし、ほぼ安定した状態で操作される場合それらを比較的長い時間の平均的な値で考えると 式(1)~(3)は皆等しいと考えられることが多く、また工業操作を議論するときには、この関係が成立するとして議論する方が妥当と考えられる。また、安定操作がなされていると見做される場合、操作過飽和度は比較的狭い範囲で操作されることが多く、特に易溶性の系の晶析操作では、式(1)~(3)の過飽和度の指数n,m,rは近似的に1とみなされることが多い。 その場合、式(1)、(2)、(3)より溶液濃度の項を消去して再整理すると式(4)が得られる。
, Ko, KD, KR, A, C はそれぞれ分子量、結晶質量、時間、総括結晶成長速度係数、拡散段階の物質移動係数、結晶表面段階の結晶成長速度係数、溶液濃度(添字b,s,I はそれぞれ溶液本体内、結晶表面温度に対応した飽和濃度、結晶表面の溶液濃度を示す)である。式(1)は結晶成長速度を総括値で表わしたものです。この現象はさらに溶質が溶液本体内より結晶表面へ拡散する段階と結晶表面に到着した溶質が、結晶格子に組み込まれる表面晶析段階に分けて考えられ、それらをそれぞれ式(2)、(3)で示した。この現象は直列機構で式(2)、(3)はそれぞれ式(1)と等しいと表示したが、速度的に考えるとその機構は全く異なりそれらは一般的には等しくない。しかし、ほぼ安定した状態で操作される場合それらを比較的長い時間の平均的な値で考えると 式(1)~(3)は皆等しいと考えられることが多く、また工業操作を議論するときには、この関係が成立するとして議論する方が妥当と考えられる。また、安定操作がなされていると見做される場合、操作過飽和度は比較的狭い範囲で操作されることが多く、特に易溶性の系の晶析操作では、式(1)~(3)の過飽和度の指数n,m,rは近似的に1とみなされることが多い。 その場合、式(1)、(2)、(3)より溶液濃度の項を消去して再整理すると式(4)が得られる。
1 / Ko = 1 / KD + 1 / KR (4 )
一方、結晶の溶解速度に対しても、2・4)の総括に従って溶解速度の関係式を結晶成長速度とアナロジーに表現すると、式(5)~(8)となる。
ム 1 / M ・dW' / d |
= Ko’A ( Cb - Cs )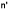 (5) (5) |
|
= KD' A ( Cb - CI )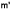 (6) (6) |
|
= KR' A ( CI - Cs ) (7) (7) |
| 1 / Ko' |
= 1 / KD' + 1 / KR' (8) |
ここで、式(5)~(8)の記号は式(1)~(4)と同じですが、上ツキ ’は溶解を意味する。 結晶成長速度および溶解速度のデータより式(1)および(5)を用いて、結晶成長速度および結晶溶解速度を求め、濃度差推進力〈 Cb- Cs 〉 に対して両対数点綴すると結晶成長速度も結晶溶解速度も濃度差推進力に対して直線関係が得られ、式(1)のnおよび式(5)のn' は共に1となった。したがって式(4)および(8)は今回のテスト結果には適用できると考えた。そこで、式(1)および(5)より、総括結晶成長速度係数および総括結晶溶解速度係数を求めた。またこのテストでは、同じ結晶を一連の結晶成長テストに用い、その後更に一連の溶解実験に使用した。そこで、同じ種晶で測定した一連のテスト結果から総括結晶成長速度係数および総括溶解速度係数を推算し、それらの値を結晶成長および溶解実験開始からデータを実測するまでに経過した時間に対して点綴すると Fig.1 が得られた。

Fig.1 中の△印は結晶成長実験に使用した種晶を溶解実験に使用したときのデータから推算した総括結晶溶解速度係数を溶解の経過時間に対して点綴したものです。溶解実験開始当初は、総括結晶溶解速度係数は総括結晶成長速度係数とほぼ同じ値であったが、溶解実験を続けているとその溶解速度は、徐々に増加し、間もなく、一定の総括結晶溶解速度係数に収束した。一方、総括結晶溶解速度係数が、一定になった結晶を結晶成長テストに使用すると、Fig.中の○印のように、暫くの間は結晶の成長速度は結晶の溶解速度と同じであったが、ある時間経過するとその結晶成長速度係数は急速に減少してほぼ一定値に収束した。このように結晶の総括成長速度係数(ここでは操作過飽和度一定で操作したときのデータであるので、この速度係数は結晶の成長速度に比例する。)が変化するのは、結晶成長速度に影響を与える結晶表面のキンクやステップ等の状況が異なるためと考える。同様に、結晶の溶解速度が変化するのも結晶表面のキンクやステップ等の影響のためである。一方拡散段階の物質移動係数は固定単一結晶の成長実験ではレイノルズの1/2乗に比例する結果を尿素添加塩化アンモニウム結晶成長の研究で得ており(この関係は 2004Bム2,2に掲載されている。)、式(4)および(8)のKD およびKD’を( 粒径/√Re )に置き換え、結晶の成長速度や溶解速度がFig. 1の一定値に収束した時の速度に着目して総括結晶成長速度係数および総括溶解速度係数を求めてその各々を( 粒径/√Re )に対して点綴すると Fig.2に示す2本の平行線が得られた。

このFig.2 中の点綴のように、総括成長速度係数と総括溶解速度係数の推算値が同じ勾配の2本の直線上にあったということは、この系の飽和濃度近傍の未飽和溶液と過飽和溶液ではその物性値は殆ど同じと考えた。そこで、Fig.2中の点綴より、流速の大きい時の総括結晶溶解速度係数を考えるとその値は、拡散段階の物質移動係数より大きく、この系では拡散段階が律速になっていると判断した。それに対して、結晶成長実験の点綴から求めた直線が縦軸と交わる切片は2.2 [ m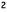 hr / m
hr / m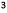 (H2O))となり、それより結晶表面段階における結晶成長速度係数を求めた。
(H2O))となり、それより結晶表面段階における結晶成長速度係数を求めた。
4) むすび
晶析実験結果と溶解実験結果を比較し、それを結晶成長機構に基づいて検討した。工業装置内結晶の成長機構や溶解機構は複雑で、ここで検討した程度の扱いで充分な説明が出来るものではない。しかし、工業操作の目的を考えると、晶析操作は工業的に評価される結晶製品を安価に安定して生産することが必要であり、市場のニーズに応える製品を生産する立場で考えると、工業操作で対象になる操作範囲で何が起っているかを知り、その操作が乱れないようにするために何をすべきか対応を十分検討しておくことが最重要である。そのためには、充分な回答が得られなくても基礎理論に矛盾にない範囲で、効率良く製品を生産できる技術を開発する努力をしなければならない。今回の検討結果は、装置内で発生する恐れのある過剰結晶核発生に対して効果的な溶解操作を提案するするうえで重要な現象を、過剰晶の除去操作を改善する時に考えやすい操作因子を中心に取り扱っており、企業現場の技術開発に参考になることが少なからずあると思う。しかし、抜本的な技術開発では、経験したことのない操作条件で技術開発を行うことは避けることが出来ない。そのよな場合には、より厳密な理論をより深く研究しておくことが大切で、それは平素から心がけるが必要である。
![]()
![]()