���_���ڎ��֖߂������z�[���֖߂���
��P�́@�Ώ̌^���_�g���A�V�� �@�@�@�@�@�@�@�@�O���Z���[���̌��������x
��P�߁@�@����
�@ �R�R�A�o�^�[�̑��`���ۂ́A�`���R���[�g�����҂ɂƂ��čł��d�v�ȕ����I
�����ł���B���̗��R�́A�R�R�A�o�^�[���`���R���[�g�ɊܗL���������̎�
������̂�����ł���(1)(2)����̂��ߍŏI���i�̗Z�_�A���A�X�i�b�v���i�p�`
���Ɗ���鐫���j�A�H���A�ۑ������̕i���͂��ׂăR�R�A�o�^�[�̑��`���ۂ�
���肳���(3)��R�R�A�o�^�[�������̌ʼn��ߒ��ɂ����镨���I�Ȗ��͑��`��
��ł���B���`����Ƃ̓R�R�A�o�^�[��ړI�Ƃ��錋�����`�Ōʼn������邽��
�̌������Ƒ��`�]�ڂł���B ���������āA�����������Ɋ֘A�����R�R�A�o�^�[
�̑��`���ۂɂ��Ă͑����̌������Ȃ���Ă���(4)-(9)� �������Ȃ���A�T�^
����Y�^(5)�ɕ��ނ����Ɨ������e���`�̕��q�\����A�������̑��x�_�A���`
�]�ڌ��ۂȂǂɂ��Ă͂܂��𖾂���Ă��Ȃ��_�������B
�@�`���R���[�g�̌ʼn��ߒ��ł́A�R�R�A�o�^�[���X�^�̑��`�Ƃ��Č���������
�邱�Ƃ��]�܂��B���̗��R�͏�q�����ŏI���i�̕i���ŇX�^���ł��D�ꂽ��
����L���Ă��邽�߂ł���B���������ă`���R���[�g���X�^�Ƃ��Č���������
�邱�Ƃ��K�v�ƂȂ肻�̂��߂ɁA�ʏ�e���p�����O���삪�s����B�e���p����
�O����ɂ���āA�`���R���[�g�Z�t���ɇX�^�̌����j�������߁A���̌�
�̗�p�H���ł��ׂẴR�R�A�o�^�[���X�^�Ƃ��Č�����������̂ł���B�Ƃ�
��ŁA���̃e���p�����O�ߒ��ŋN�����Ă��錻�ۂɂ��ẮA���𖾂ȕ�����
�����B
�@�e���p�����O����͋�̓I�ɂ́A�Z�t�`���R���[�g�i�U�O���j���Q�V���t��
�܂ŝ��a���Ȃ����p�����̌�R�P���ɂ܂ŏ�������P�ʑ���ł���B�]���e
���p�����O����ŋN���錻�ۂƂ��āA��p�r���ʼnߗ�p�x�̑傫���Z�_�̍���
���`�����������A���̌�̏����ߒ��łR�P���ȉ��̗Z�_�������`���Z������
���߂ɁA����ȇX�^�̌����j��������ƍl�����Ă������A�ߗ�p�x�Ɗe��
�`�̌������̊������G�l���M�[�ɂ��Ă̍l�@�͍s���Ă��炸�A�K��������
��p�x�̑傫�����`���͏o����Ƃ͌���Ȃ����̂Ǝv����B
�R�R�A�o�^�[���܂߂āA�V�R�����ł�������͎�X�̃g���A�V���O���Z���[
���̍������ł���B���̂悤�Ȗ����̕����́A���̍\���g���A�V���O���Z���[
���̌X�̕����I�����Ɉˑ����A���̏�ō\���g���A�V���O���Z���[���̕��q
�ԑ��ݍ�p�Ō��肳�����̂ƍl������B����A�\���g���A�V���O���Z���[
���ɂ͓Ǝ��̑��`���ۂ����݂���B���Ȃ킿�A�X�̃g���A�V���O���Z���[��
�̑��`�̔M�͊w�Ƒ��x�_�Ɋւ���m���̒~�ς��Ȃ���A���q�ԑ��ݍ�p��
�����邱�Ƃ͍���ł���B
�@�ȏ�̂��Ƃ���A�R�R�A�o�^�[�̑��`���ۂ����S�ɗ������邽�߂ɂͤ�܂��R
�R�A�o�^�[�̎听���̃g���A�V���O���Z���[���Ɋւ��錋�������w�I�Ȓm����
�K�v�ł���B�R�R�A�o�^�[�̎听���g���A�V���O���Z���[���ͤ�o�n�o��o�n�r�
�r�n�r�ł���A������� 2-�ʂɃI���I�C�������������Ă��邪������� 1,3-
�ʂɓ������b�_����L����u�Ώ̌^�v�i�o�n�o�A�r�n�r�j�ƈقȂ鎉�b�_����
�L����u��Ώ̌^�v�i�o�n�r�j�Ƃɕ��ނ����B�o�n�o�Ƃr�n�r�̑��`���ۂ�
�M�͊w�I�E�\���_�I������ Sato��ɂ���ďڍׂɉ𖾂��ꂽ(10)�
�@�{�͂ł́A�R�R�A�o�^�[�̍\���g���A�V���O���Z���[���̒��ŁA�u�Ώ̌^��
�_�g���A�V���O���Z���[���v�ł���A�o�n�o�Ƃr�n�r�̌����������A���Ɍ���
�����x�_�q�ԑ��ݍ�p�̊�b�Ƃ��Ę_����(11)(12)�
��Q�߁@����
2�1�@��������я��x�̌���
�@�{�����ɗp�����o�n�o�A�r�n�r�͕s����������ꂽ�B�@���x��99%��
����A����t�̃N���}�g�O���t�B�[�ɂ���Đ����������̂ł���B
���x�̌���́A�g�o�k�b�ɂ��ȉ��̕��@�ōs�����B
�@�J�����FLichrosorb RP-18(Merck),5��m,4.6�Ӂ~25�p
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�Q�{����
�@�@�@�@A-303 ODS(Yamamura Chemical Lab.),5��m,4.6�Ӂ~25�p
�@�n�@�}�F�A�Z�g���^�A�Z�g�j�g�������V�V�^�Q�R�i�e�ϔ�j
�@�� ���F�A�Z�g�����ɁA�T���Z�x�ŗn���iwt/vol�j
�@�����ʁF�P�O��l�@
�@�n�o���x�F�PmL�^���@
�@��щ��x �F�R�T��
�@���o��@�F�������܌v�i���Ð��쏊�ARID-6A�j
2�2�@�w�����
�@�����\���͍L�p�����w����ܖ@�ɂ�葪�肵���B�w����ܑ��u�Ƃ��ė��w�d
�@�q�`�c�|�U�b�^�i�bu�j���G40KV,20mA�A�O���t�@�C�g���m�N�����[�^�����j
��p�����B�����̓K���X�����i�[��0.3�o�j�ɕ\�ʂ������ƂȂ�悤�ɏ[�U���A
�Q��=1�`30deg�܂łUdeg/���ő��������B�w����ܑ���̏I����������DSC��
�͂̂��߂ɃK���X�������璼�ڃT���v�����O���A���ꎎ���łw����c�r�b����
����s�����B
2�3�@�c�r�b
�@�c�r�b���u�̓Z�C�R�[�d�q�H�Ƃq�c�b�Q�^���g�p���A���x����їZ���G���^
���s�[�̕W���Ƃ��ăK���E����p�����B������P�������A���~�j�E�����p����
���ʂ��A�t�̒��f��p����-�Q�O���ɗ�p�����Ă��珸�����x�Q�O���^���ő���
�����B
2�4�@���`�̓���
�@�o�n�o�A�r�n�r�̑��`���ۂ� Sato��(10)�ɂ���ďڍׂɌ�������Ă���B
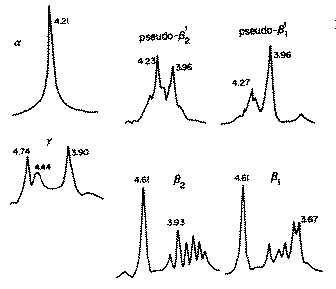
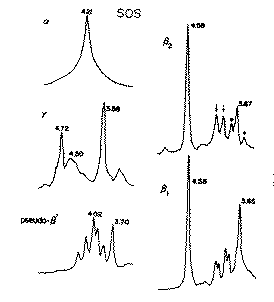
�@Fig.1-1�ɂ͂o�n�o�Ŋm�F���ꂽ�U���`�̂w����܃X�y�N�g�����AFig.1-2��
�͂r�n�r�Ŋm�F���ꂽ�T���`�̂w����܃X�y�N�g���������B�{�����œ���ꂽ
�����̑��`����͂����̃X�y�N�g���Ƃ̔�r�A�܂��M�I�ȃf�[�^����������
���Ƃɂ���čs�����B
 |
 |
2�5�@���������x
�@���������x���葕�u�� Fig.1-3�Ɏ����B�{���u�͕Ό�������������������
�̂ł���B
�@���̑��u�́A�Ό��������̑Ε������Y���O���ڊ���Y�ɂb���r���Z���T�[
�����t�������̂ł���B�����͍P�����̗����K���X�Z����ɂ����A0.3�o��
�x�̃X�y�[�T�[������ŃJ�o�[�K���X�������Ă���B�Ό��q�ƌ����q�̓N���X
�j�R���ƂȂ�悤�ɃZ�b�g����Ă���̂ŁA�������������Ȃ�������������
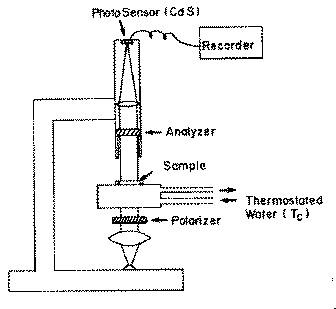 |
���͐ڊ���Y�����i���Z���T�[�j�ɂ͓��B���Ȃ��B�P�������͂Q��p�ӂ���
����A���H��d���قŐ�ւ�����B�K���X�Z���𗬂��P�������A������
���x�iTc�j�ɒ��������P�����ɐ�ւ���ƁA���̑҂����ԁi�сj�̌�A��
���̌��������n�܂�B�������Ɠ����ɁA��������̌��͌��w�I�Ɉٕ��I�ȃg��
�A�V���O���Z���[�������ɂ���đȉ~�Ό����̍�p���邽�߁A�Z���T�[��
���ɓ��B�ł���悤�ɂȂ�̂ŁA��������o���邱�Ƃ������Ƃ��Č������̑�
�����Ԃ𑪒�ł���B�b���r�ɂ̓o�C�A�X�Ƃ��ĂP.�T�u��������A����ɂ��
��R�ω������u�P�ʂœǂ݂������B�Ȃ��P�����̗��H��ւ��p�d���ق����
���Z���T�[�̌��o�M���̓p�[�\�i���R���s���[�^�iNEC;PC9801�j��GP-IB
�C���^��t�F��X����Đڑ����ꂽ�}���`�v���N�T-(Hewlett�@Packard
�g�o3497A�j�A�f�W�^���}���`���[�^�[�iYokokawa;2502A)�ɂ���Đ���A
�f�[�^���W�����V�X�e�����\�z�������ɋ������B���W���ꂽ�f�[�^�́A���C
�}�̂ɕۑ��\�œK�X�f�[�^�����A��͂��ł���B
�@�Ε������Y���O�������R�́A�����̑S����Ď��ł���悤�ɂ��邽�߂ŁA����
�ɂ�蕔���I�ɐ͏o�������������ׂČ��o�ł��邱�Ƃ��m�F���ꂽ�B
2�6�@���������@
�@���������@�Ƃ��ĂQ��ނ̎������@�A���Ȃ킿
�@�@�@�@�P����p�isimple cooling�j
�@�@�@�@�Z�t�}������imelt-mediation�j
���s�����B
�@�P����p�́A�����g���A�V���O���Z���[�����W�O���ŗZ�����A���̌�K���X
�Z���̉��x�����������x�iTc�j�ɐ�ւ�����@�ł���B
�@�Z�t�}������ł́A�K���X�Z�����x���A���߂ɐ��������������`�̗Z�_��
��̉��x�}���ɏ㏸�����邱�Ƃɂ���Č�����Z�������A���̌�ɐ͏o����
������ȑ��`�̏o�����ϑ�������@�ł���B�Z�������錋�����`�Ƃ��āA��
�^�ƃ��^���g�p�����B���G�ȑ��`���ۂ������g���A�V���O���Z���[���ɂ�����
�́A�Z�t�}����������葽�`������L���ȕ��@�ł��邱�Ƃ��m���Ă�
��(12)�
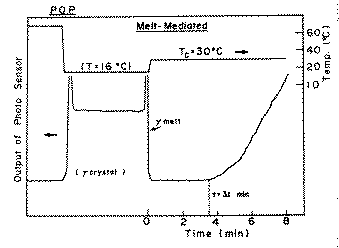
�@Fig.1-4�ɂ́A�o�n�o�̒P����p�ł̓T�^�I�Ȍ������������������B���̐}��
�́A�Q��ނ̈قȂ錋�������x�iTc�j�ł̌������Ȑ����`����Ă���B
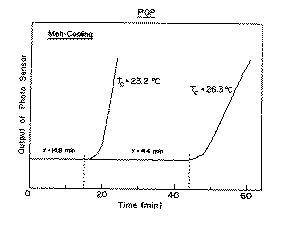 |
�@�@�@�@�@POP at Tc=23.2 and 26.3��.
Tc=�Q�R.�Q���ł͂P�S.�W���܂Ō��Z���T�[�̏o�͂ɕω��͔F�߂��Ȃ����A��
�̌�}���ȏo�͑��傪�ϑ������B����͌������̎n�܂�ƌ���������������
����A���̏ꍇ�������̑҂����Ԃ́A��=14.8���ƒ�`�����B ���l�ɁATc=
�Q�U.�R���ł́A��=44���ł���B
�@Fig.1-5�ɂ́A�o�n�o�̃�-�Z�t�}������̓T�^�I�ȗ�������B�����菇��
�ȉ��Ɏ����ʂ�ł���B�͂��߂ɁA�U�O���̗Z�t���P�U���ɋ}�₷��B���̑�
��ɂ���ă��^�������������邪�A����͐}�̋}���Ȍ��Z���T�[�o�͂̑����
����Ă���B���炭����ƌ��Z���T�[�o�͂͌������邪�A����͎����S�̂�
 |
�@�@�@�@�@�@crystallization of POP.
�������������Ƃɂ���Č����U�����A��������̓��ߗʂ������������߂ł���B
���������^�Ƃ��Ă��ׂČ��������Ă���T����ɁA�K���X�Z�����x���R�O����
�Ƌ}���ɏ���������B���̑���ɂ���Đ͏o���Ă��������͂��ׂėZ������B
����́A���Z���T�[�o�͂̋}���Ȍ����ɔ��f����Ă���B����̓��^�̗Z�_��
�Q�V���ł��邽�߂ł���B���̌�pseudo-��'1�^��pseudo-��'2�����̌��������x
�iTc=�R�O���j�Ő͏o����B���̏ꍇ�A����Z�t�}������ɂ�錋�����҂���
�Ԃ́A��=�R.�P���ƒ�`�����B���l�ȕ��@�ŁA��-�Z�t�}������̑҂�����
�𑪒肵���B
�@
��R�߁@��������
3�1�@�o�n�o
�@�R��ނ̈قȂ錋�������@�ɂ���Đ͏o���鑽�`�� Table 1-1�Ɏ����B
Table 1-1 Occurrence of POP Polymorphs in Melt Crystallization
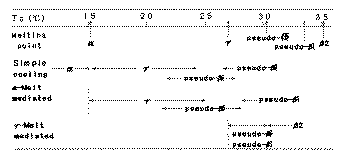 |
�@�P����p�������ł́A���^�̐͏o�Ɋւ��ĉߗ�p���ۂ͔F�߂��Ȃ������B
���Ȃ킿�A���^�͂��̗Z�_�����Ō����������B���^�́A���^�̗Z�_����Q�S��
�܂ł͈̔͂�Tc�Ō����������B�܂��Apseudo-��'2�͂Q�R������Q�V���܂ł̔�
�͂ŁApseudo-��'1�͂Q�V���ȏ�Ő͏o�����B26������27���̊Ԃł͗����̑�
�`���o�������B�����2��ނ�pseudo-��'�̏o���́A�ő��]�ڂ̉ߒ��ł��F�߂�
��Ă���(10)������̌��ʂ���A�o�n�o�ɂ͂Q��ނ�pseudo-��'�^�����݂���
���Ƃ��ؖ����ꂽ���ƂɂȂ�B
�@��-�Z�t�}������ł́A���^�̗Z�_�ƂQ�S���Ƃ̊ԂŃ��^�������������B
pseudo-��'2�^��22���t�߂���͏o���͂��߁A���������x�������Ȃ�ɂ�āA
pseudo-��'1�����ꂽ�B�����ĂQ�W���ȏ�ł�pseudo-��'1�݂̂�����ꂽ�B
�@����Z�t�}������ł́A���^�̗Z�_�ȏ�31���܂ł͈̔͂ŁApseudo-��'2�^
��pseudo-��'1�^�̗��҂��͏o�����B31���ȏ�͈̔͂ł́A��2�^�݂̂�����ꂽ�B
���������P�^�̌������͔F�߂��Ȃ������B
�@Fig.1-6�ɂ͒P����p�������ɂ����錋�����҂����ԁi�сj�̋t���̉��x�ˑ�
�����������B1/�т͌��������x�ɔ�Ⴗ�鐔�l�ł����BTc���Q�P���͈̔͂ł�
���^�ƃ��^�Ƃ��͏o�������A�����̌��������x�͑傫�����āA�Z���̑��u��
�������������������߂��̐}�ɂ͎�����Ă��Ȃ��BFig.1-6���疾�炩�Ȃ悤
��1/�т�pseudo-��'1���ł��������A�����ł��傫���B�����̌��ʂ���A������
���x�̓��^���ł������Apseudo-��'1�^���ł��x���ƌ��_�ł���B
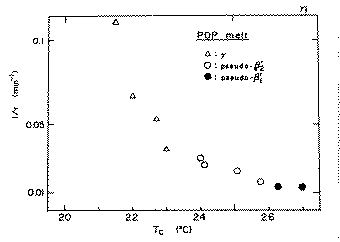 |
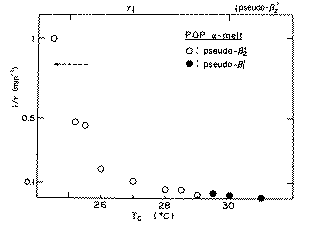
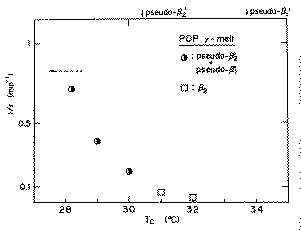
Fig.1-7�ɂ̓���Z�t�}������ɂ����錋�������x���������B�Z���̑��u��
���͐}���̖��ŕ\����Ă���B���^�ɑ���1/�т͑傫�����Đ��m�ɑ����
���Ȃ����߁A�}������Ă��Ȃ��Bpseudo-��'2�ɂ�����1/�т͏��pseudo-��'1
�̂��̂����傫�Ȓl���������B����Ƀ���Z�t�}������ɂ����錋�������x�́A
�P����p�������ł̑��x�Ɣ�r����ƂP�O�{�������Ƃ��킩��B���̂��Ƃ���A
���^�̗Z���̌�ɋN���錋�����̑��x�́A�P����p�̏ꍇ����������������
��邱�Ƃ����炩�ƂȂ����B
 |
�@�@�@�@�@�@crystallization of POP.
�@Fig.1-8�ɂ� ����Z�t�}������ł̌��������x�̉��x�ˑ������������B��-
�Z�t�}������Ƃ͂R�̓_�ő��Ⴊ�F�߂�ꂽ�B
(1)1/�т̒l�́A����̉��x�Ŕ�r����ƃ�-�Z�t�}������̕����A��-�Z�t
�@�@�}����������P�O�{�̑��x���������B
(2)28������30���͈̔͂ɂ����āA����Z�t�}������ł�pseudo-��'2�^��
�@�@pseudo-��'1�^�Ƃ������Ɍ������������A����Z�t�}������ł͂�����
�@�@�Q�X���t�߂����Ƃ��ĕʌɏo�������B
(3)����Z�t�}������ɂ���ă�2�^�������������B
 |
�@�@�@�@�@�@crystallization of POP.
3�2�@�r�n�r
�@�o�����`�̌��ʂ� Table 1-2 �Ɏ������B
Table 1-2 Occurrence of SOS Polymorphs in Melt Crystallization
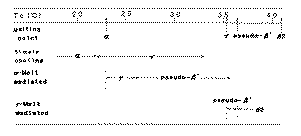 |
�@�P����p�������ł́A���^�ɂ��ĂQ.�T���̉ߗ�p���ۂ��F�߂�ꂽ�B����
�킿���^�͂��̗Z�_�ȉ��̂Q�P���Ő͏o���J�n�����B���^�͑��̑��`�Ɣ�r��
�Ĕ��ɍL�����x�͈́i�Q�P�`�R�R���j�Ō����������B
�@����Z�t�}������ł́A���^�̗Z�_�ȏ�Q�U���܂ł͈̔͂ŁA���^�̌�����
��U�������B�������A����ȏ�̉��x�̈�ł͍L���͈͂ɂ킽���� pseudo-��'
�^������A�o�n�o�̏ꍇ�Ƃ͎�قȂ�X��������ꂽ�B�܂�A��-�Z�t�}��
�������ł͂Q�U���ȏ��pseudo-��'�^�������������B
�@�o�n�o�̏ꍇ�Ɠ��l�ɁA��2�̓�-�Z�t�}������ɂ�����pseudo-��'�̗Z�_
�ȏ�̉��x�Ō����������B
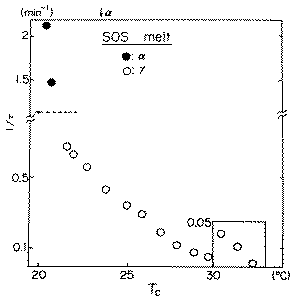
�r�n�r�̒P����p�ɂ�����1/�т� Fig.1-9�Ɏ������B�}���̖��́A�Z���̑�
�u�萔��\���Ă���B�Q�Q���ȉ��ł̓��^�����ɑ����͏o���A�т͑��u�萔
�����������i1/�т��傫���j�B���^�́A���^�̗Z�_�ȉ��̗̈悩��R�Q����
�ł͈̔͂Ő͏o�����B�r�n�r�̒P����p�������ł́A�����ȊO�̑��`�̐͏o
�͂R�Q���ȉ��ł͔F�߂��Ȃ������B
�@Fig.1-10�ɂ́A�r�n�r�̃���Z�t�}��������x���������B���̌��������@��
�́A���^�͂����P�̉��x�ɂ����Ă̂ݓ���ꂽ�Bpseudo-��'�^�͔��ɍL����
�������x�͈͂Ő͏o�����B�����f�[�^������Ă���̂͌��������x�������A��
�����u�萔�ȉ��ł��邽�߂ł���B
 |
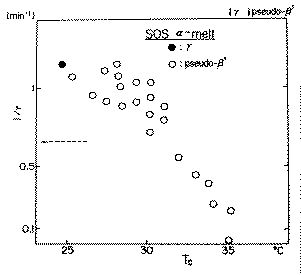
�@����Z�t�}������łͤ���^�̗Z�_��pseudo-��'�^�̗Z�_�Ƃ̊ԂŤpseudo-��'
���͏o�����B��2�^�͔��ɒ����i�W�O���ȏ�j�҂����Ԃ̌�Ɍ����������B
 |
�@�@�@�@�@�@�@crystallization of SOS.
��S�߁@�l�@
�@�{�������ʂ��POP�ɂ��Ă̓�����pseudo-��'2�pseudo-��'1���2�^�̂T��
�̑��`���A�r�n�r�ɂ����ẮA������pseudo-��'���2�^�̂S��ނ̑��`�̑��݂�
�ؖ����ꂽ�BPOP�̔��ɕ��G�Ȓ��ԑ��`�ł���pseudo-��'2�^��pseudo-��'1�^
�Ƃ͂R��ނ̌��������@�ŒP��̑��`�Ƃ��ē��肳��A����炪�Ɨ�������
���`�ł��邱�Ƃ��m�F���ꂽ�B����́ASato��ɂ�錋���]�ڂ�p�������_��
��v���Ă���(10)���1�^�͖{�͂ň������Z�t����̌������ł͓����Ȃ�����
���AArishima��̌��ʂɂ��ƁA�n�t����̌������ɂ���ă�2�^�Ƌ��ɐ͏o��
��Ă���(13)��Z�t����̃�1�^�̐͏o�ɂ͔��ɒ������Ԃ�v������̂Ɛ���
�����B �@�{�͂œ���ꂽ���ʂ̒��ŋ����[���_�́A�o�n�o�ł̓��^�ɉߗ�p���ۂ��F
�߂��Ȃ��������A�r�n�r�ł̓��^�����^�̗Z�_�ȉ��Ō����������_�ł���
�iTable 1-1, Table 1-2�j�B�@�@�܂�A���^�͂Q�����\���ł��邱�Ƃ���A
�o�n�o�̕����r�n�r�ɔ�ׂĂQ�����\���Ō��������₷�����Ƃ������Ă���
�iFig.1-11�j�B���̌����̓g���A�V���O���Z���[�����\�����Ă��鎉�b�_����
 |
����l�@�����B�o�n�o���̃p���~�g�C�����ƃI���I�C�����̒����͔��ɋ�
���B�Ȃ��Ȃ�I���I�C����������cis-��d�����ɂ���ċ��Ȃ��Ă��邽�߂�,
�S�̂̍����Ƃ��Ă̓p���~�g�C�����Ƃقړ������Ȃ邩��ł���B����A�I��
�I�C�����ƃX�e�A���C�����Ƃ����ꃉ�����ɔz�������ꍇ�A�X�e�A���C������
�����������߂Ƀ������ʂ������i�A�V�������[���X�e�A���C�����ɂ����ē�
�o����j�B���̂��߁A���^�����̈��萫�͂o�n�o�̕����傫���B�����A�o�n�o
�̃��^�̗Z���G���^���s�[�i���g��=68.1KJ/mol�j�̕����A�r�n�r�i��:���g��=
47.7KJ/mol�j�����������傫���l�������Ă���(10)���q�̍l�@�𗠕t��
�Ă�����̂ƍl������B
�@���������x�Ɋւ��ẮA�s����ȑ��`�͂�����ȑ��`�Ɣ�r���ď�ɑ���
�Ȃ�Ƃ������ʂ̌��ʂ��������B����͎����ɗp�����R��ނ̌��������@�̂�
�ׂĂœ��l�̌��ʂł������B�������̑҂����ԁi�сj�́A�j�����̗U�����Ԃ�
���������U�����Ԃ̗��҂��܂�ł���B�j�������x�͉ߗ�p�x���傫��������
�Ȃ邪���������Ƌt��Ⴕ�Ĕ��������j�̊E�ʃG�l���M�[�͏������Ȃ�(14)
����̌��ʂ́A������ȑ��`�̊E�ʃG�l���M�[���s���葽�`�����傫������
�������Ă���B���l�ȍl�@�́A�g���p���~�`���̃�'����у��^�ɂ����ċc�_��
�����(15)�
�@ �@�����ɗp�����R��ނ̌��������@�ɂ��Ⴂ���r�������ʁA�ȉ��̓_����
�炩�ƂȂ����B
�@(1)���������x�̓���Z�t�}������E����Z�t�}������̕����P����p����
�@�@ ���ɔ�r���āA���������������B
(2)�o�����鑽�`�̋��������������@�ɂ���ĈقȂ��Ă����B���Ƀ���Z�t�}
�@�@������͒P����p�A����Z�t�}������ƈقȂ鋓�����������B
���̓_�Ɋւ��Ă̓g���p���~�`���̗Z�t����̃��^�A��'�^�̌������ɂ�����
���l�̌��ʂ������Ă���(15)��Z�t�}������́A�����j�╪�q�W���̂̑�
�݂ɂ���Č����������i����邱�Ƃ��e�Ղɑz�������B�����̊j�╪�q�W
���̂́A���^����^�Ȃǂ̂͂��߂ɑ��݂��Ă������`���A�}���ȏ�������ɂ�
���ėZ������ۂɐ���������̂ł��낤�B���̂悤�ȋ@�\���A��-�Z�t�}���
�������Z�t�}������ŋN�����Ă�����̂Ǝv����B
�@����ɁA����Z�t�}������̕����A����Z�t�}����������傫��������
���x���������B���̌����́A���^�̗Z����ɐ����錋���j�i�܂��͕��q�W���́j
����r�I���₷���s����Ȃ��߂ƍl������B�Ȃ��Ȃ�A���^�͍ł��K��
���ɖR�������`�ł��邩��ł���(16)����������āA�������������x�ɂ�����
����Z�t�}������ߒ��́A�s����^�ł��郿�^�����S�ɑ��₩�ɗZ�����邽��
�ɁA�����j���c�������邱�Ƃ��Ȃ��A���ʂƂ��ĒP����p�������Ɨގ�������
�̂ƂȂ���̂ƍl������B
�@���l�̍l�@�́A��-�Z�t�}������ɂ����p�ł���B���Ȃ킿�A���^�̗Z����
����Đ������錋���j�╪�q�W���̂́A����Z�t�}������̏ꍇ��������
��ȑ��`�̊j�ƂȂ�B���̌��ʁA��������������`�^������Z�t�}������ɂ�
���ē���ꂽ���̂ƍl���邱�Ƃ��ł���B
�@�Ō�ɁA�{�͂œ���ꂽ���ʂ��R�R�A�o�^�[�̌������ߒ��Ƃ̊֘A�Ř_�l��
�邱�Ƃ��ł���B�`���R���[�g�̌ʼn��ߒ��ł́A�{�����ōs��ꂽ�悤�ȗZ�t
�}��������N�����Ă�����̂ƍl������B�Ȃ��Ȃ�A�`���R���[�g����
�̐����H���ōŏ��Ɏ�M�I�����́u�e���p�����O(��������)�v�́A�Z�t�`
���R���[�g���}���ɗ�p���邱�Ƃ����̑��i�K�ł��邩��ł���B���̒i�K
�ŁA�`���R���[�g���̃R�R�A�o�^�[�ɂ͕s����ȑ��`�������Ă��邱�Ƃ��m�F
����Ă���(17)����������e���p�����O�i�K�͏����ߒ��ł��邪�A�����Ő���
�����s���葽�`���Z�����A����Ɠ����ɂ�����ȑ��`���͏o����i�Z�t�}��
�������j���̂Ɛ��������B�`���Ř_�����悤�ɁA�ŏI���i�̃`���R���[�g��
�ɑ��݂���R�R�A�o�^�[�̑��`�͇X�^�ŁA���̌����^�͂o�n�o��r�n�r�̃�2�^
�Ɉ�v���鑽�`�ł���B���������� ��2�^��͏o������悤�ȔM�I���������A��
�Ȃ킿�o�n�o��r�n�r�ŔF�߂�ꂽ�悤�ȃ�-�Z�t�}��]�ڂ��N����悤�ȏ���
���A�`���R���[�g�̒��������ɂ����čœK�ł�����̂Ƃ�����B�Ȃ��A�R�R�A
�o�^�[�������Ɋւ�����[���l�@�́A���͂ŏq�ׂ�o�n�r�̌����������A��
�R�͂ŏq�ׂ� �o�n�o/�o�n�r/�r�n�r �R�����n�̌��ʂ��܂߂��l�@���K�v��
����B
��T�߁@�@�܂Ƃ�
�����x�̎�����p���āAPOP�̂T���`�i���A���Apseudo���'2�Apseudo-��'1�A��2�j
����тr�n�r�̂S���`�i���A���Apseudo-��'�A��2�j�̗Z�t����̌��������s�����B
�Z�t���Ɍ������͏o����܂ł̑҂����ԁi�сj���A�P���Z����Ɏ������悹�A
���Z���T�[�������Ό���������p���đ��肵���B���������x��1/�тɂ��
�Ē�`���A���`�̓���͂w����ܑ��u����тc�r�b�ɂ��s�����B
�@���������@�Ƃ��āA�P����p�������E�Z�t�}������i��-�A��-�j��p����
���o�n�o�Ƃr�n�r�łقړ��l�̌��ʂ�����ꂽ�B
�@(a)���������x�͕s���葽�`�ɂ����ď�Ɉ��葽�`�������������B�܂��A��2
�@�@�^�̏o���̓���Z�t�}��]�ڌ������ɂ���Ă̂݊ϑ����ꂽ�B��1�^�̐͏o
��
�@�@�F�߂��Ȃ������B
�@(b)���ꌋ�������x�ɂ����āA�Z�t�}������ł̌��������x�͏�ɒP����p
�@�@�������������������B
�@(c)���`�̏o�������͒P����p�ƗZ�t�}������ňقȂ��Ă����B
�����̌��ʂ��R�R�A�o�^�[�������̋@�\�Ɗ֘A�����čl�@�����B
����
1. R.E.Timms, Prog. Lipid Res., 23, 1 (1984).
2. G.G.Jewell, in Industrial Chocolate Manufacturing
and Use,
�@�@ed. by S.T.Beckett, Blackie & Son Ltd., Glasgow, p.227, (1988).
3. F.R.Paulicka, Chem. Ind. (London), 17, 835 (1973).
4. R.O.Feuge, W.Landmann, D.Mitcham and N.V.Lovegren,
�@�@J.Am.Oil Chem.Soc.,39,310 (1962).
5. R.L.Wille, E.S.Lutton, J.Am.Oil Chem.Soc., 43,491
(1966).
6. A.Huyghebaert and H.Hendrickx,Lebensm. Wiss. Techn.
4,59 (1971).
7. J.D.Hicklin, G.G.Jewell and J.H.Heathcock, Food
Microstructure,
�@�@4,241 (1985).
8. P.S.Dimick and T.R.Thomas, J.Am.Oil Chem.Soc.,64,1663
(1987).
9. J.Schlichter-Aronhime and N.Garti, in Crystallization
and
�@�@ Polymorphism of Fats and Fatty Acids, ed. by N.Garti and K.Sato,
�@�@ Marcel Dekker, New York, p.363 (1988).
10. K.Sato, T.Arishima, Z.H.Wang, K.Ojima, N.Sagi
and H.Mori,
�@�@J.Am.Oil Chem.Soc., 66,664 (1989).
11. T.Koyano, I.Hachiya, T.Arishima, K.Sato, N.Sagi,
�@�@J. Am. Oil Chem. Soc., 66:675 (1989).
12. T.Koyano, I.Hachiya and K.Sato, Food Microstructure,
9:231 (1990).
13. T.Arishima and K.Sato, J.Am.Oil Chem.Soc., 66,1614
(1989).
14. R.Boistelle,in Crystallization and Polymorphism
of Fats and Fatty
�@�@Acids, ed.by N.Garti and K.Sato,Marcel Dekker, New York,p.189(1988).
15. K.Sato and T.Kuroda, J.Am.Oil Chem.Soc.,64,124
(1987).
16. K.Larrson, Ark.Kemi, 23,35 (1964).
17. I.Hachiya, T.Koyano and K.Sato, Yukagaku, 37,
431 (1988).
���_���ڎ��֖߂������z�[���֖߂���