倫俫丏俲俫偲僇儖僔僂儉
丂倫俫丄俲俫偲僇儖僔僂儉偼儕乕僼傾僋傾儕僂儉偱崅傔偺抣傪堐帩偟偨偄崁栚偱偡偑丄俁幰傪摨帪偵崅偔偡傞偙偲偼晄壜擻側偨傔丄擸傓偙偲偑偁傝傑偡丅偙偙偱偼丄俁幰偺娭學偵偮偄偰彂偄偰傒偨偄偲巚偄傑偡丅
俙乯幙検嶌梡懃
丂俙亄俛佁俠亄俢偺斀墳宯偑偁傞偲偒丄俙傑偨偼俛傪壛偊傟偽俙亄俛仺俠亄俢偲俙丄俛傪傊傜偡曽岦偵斀墳偑恑傒丄媡偵俠丄俢傪壛偊傟偽俙亄俛仼俠亄俢偺曽岦偵斀墳偑恑傒丄俠丄俢傪尭傜偦偆偲偟傑偡丅偙傟偑幙検嶌梡懃偱偡丅
丂娚徴嶌梡傕幙検嶌梡懃偵傛偭偰偍偒傑偡丅
俛乯倫俫
丂悈慺僀僆儞擹搙丗乵俫+乶偼倫俫偱帵偝傟傑偡丅倫俫=-log乵俫+乶偱偡丅
偮偹偵丄log乵俫+乶亄log乵OH-乶=14偲偄偆娭學偑偁傝傑偡偐傜丄倫俫俉偺帪丄乵俫+乶偼10-8mol/l丄乵OH-乶偼10-俇mol/l偱丄悈巁婎僀僆儞偼丄悈慺僀僆儞偺100攞懚嵼偟傑偡丅
丂倫俫8.6枠忋徃偟偰傕僒儞僑偵偼埆塭嬁偑偁傝傑偣傫偑丅憯椶偼擇巁壔扽慺傪媧廂偱偒側偔側傝丄徚柵偟偰偄偒傑偡丅
俠乯俲俫
丂扽巁墫峝搙乮Carbonate丂Hardness乯俲俫偼傾儖僇儕検丄巁拞榓擻傪帵偟傑偡丅d俲俫傪2.8偱妱傟偽丄meq/l偲側傝傑偡丅
倫俫偲俲俫丄嬻婥拞偺擇巁壔扽慺偵偼埲壓偺娭學偑偁傝傑偡丅
丂丂丂丂丂丂丂丂倫俫=倫俲亄log乵HCO3-乶/乵H2CO3乶
丂丂丂丂丂丂丂丂丂丂=6.1亄log乵HCO3-乶/兛PCO2
丂丂丂丂丂丂丂丂丂丂=6.1亄log乮俲俫/2.8乯/0.0301丒PCO2ゥ@
偙偙偱丄
倫俲丗廳扽巁僀僆儞偺摍揹揰乮H2CO3偲HCO3-偑摍偟偔側傞倫俫乯
兛丗擇巁壔扽慺暘埑偐傜丄梟夝偡傞meq/l傊偺曄姺學悢乮0.0301乯
PCO2丗嬻婥拞偺擇巁壔扽慺暘埑
懠偺僀僆儞偺塭嬁傕偁傝傑偡偺偱丄偙傟偩偗偱丄倫俫偺寁嶼偼偱偒傑偣傫偑丄嘆幃偐傜尵偊傞偙偲偼丄倫俫偲俲俫偼嬻婥拞偺擇巁壔扽慺検偵嫮偔塭嬁傪庴偗傞偲偄偆偙偲偱偡丅姺婥偑埆偔丄僸僩偺屇婥拞偺偵巁壔扽慺偱幒撪偺擇巁壔扽慺暘埑偑崅偄偲倫俫偼崅偔側傝傑偣傫丅
丂奀悈偺昗弨揑俲俫偼俉倓俲俫偱偡丅俇倓俲俫傑偱偼僴乕僪僐乕儔儖偼塭嬁傪庴偗傑偣傫偑丄傗傗愇奃憯偺惗堢偼埆偔側傝傑偡丅俆倓俲俫偵側偭偨傜曗惓傪偟側偄偲媫懍偵倫俫偑掅壓偡傞偙偲偑偁傝傑偡丅乮屻偱弎傋傑偡偑丄悈巁壔僇儖僔僂儉揧壛埲奜偺尨場偱俲俫偑棊偪偨偲偒乯
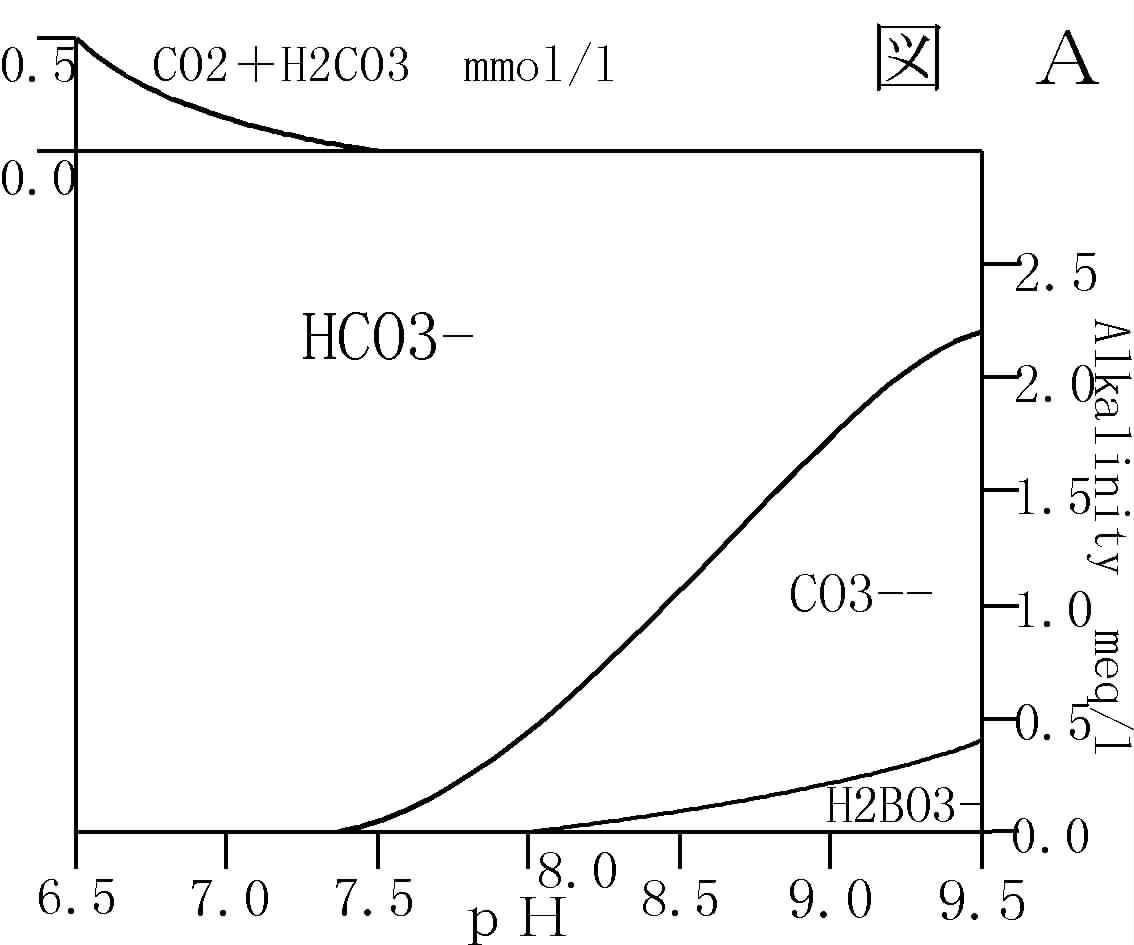
丂CO2亄H2O佁H2CO3佁俫+亄HCO3-佁俀俫+亄CO3--
偲擇巁壔扽慺偼倫俫偵傛偭偰偦偺懚嵼宍懺傪曄偊傑偡丅倫俫偑8.5傪墇偊偰媫偵忋徃偡傞偲偲丄僇儖僔僂儉擹搙偑媫寖偵壓偑傞偺偼丄CO3--偑憹偊丄偙傟偲捑揳偟偰偟傑偆偨傔偱偡丅
丂丂丂丂丂
丂偙偺棟桼偵傛傝丄崅倫俫丄崅俲俫偲崅僇儖僔僂儉忬懺偼偁傝摼側偄偺偱偡丅
乮懠偺巁偑憹偊偨傝偟偨偲偒偼丄掅倫俫丄掅俲俫偲掅僇儖僔僂儉忬懺偼婲偙傝摼傑偡偑丅乯
俢乯僇儖僔僂儉
丂捠忢偺奀悈偵偼420mg/l娷傑傟偰偄傑偡丅僒儞僑傗愇奃憯偺媧廂丄僾儘僥僀儞僗僉儅乕偵傛傞夞廂偵傛偭偰丄悈憛拞偺僇儖僔僂儉偼彊乆偵幐傢傟偰偄偒傑偡丅偙偺偨傔丄帩懕揑側僇儖僔僂儉曗媼偑儕乕僼傾僋傾儕僂儉偵偍偄偰偼昁梫偲側傝傑偡丅
侾乯Kalkwasser偵傛偭偰壛偊傞応崌
丂媡怹摟枌側偳偱張棟偟偨悈侾儕僢僩儖偵懳偟偰丄1.26g埲忋偺悈巁壔僇儖僔僂儉丗Ca乮俷俫乯2傪梟偐偟丄偦偺忋悷傒傪揰揌搳梌偡傞曽朄偱偡丅揰揌搳梌偡傞棟桼偼丄堦婥偵壛偊傞偲媫寖側倫俫忋徃傪彽偒丄扽巁僇儖僔僂儉偺捑揳偲側偭偰偟傑偆偨傔偱偡丅
丂Kalkwasser搳梌偵傛傝丄崅倫俫偲崅僇儖僔僂儉偑傕偨傜偝傟傑偡偑丄俲俫偼傗傗掅傔偲側傝傑偡丅偙傟偼丄僇儖僔僂儉偵傛傝扽巁偑彮偟捑揳偟偰偟傑偆偨傔偱偡丅偙偺帪偵丄俲俫忋徃嵻傪壛偊傞偲崱搙偼僇儖僔僂儉偺捑揳偑憹壛偟丄僇儖僔僂儉擹搙傪壓偘偰偟傑偄傑偡丅俲俫偑俇倓俲俫偖傜偄傑偱偼丄俲俫忋徃嵻傪巊傢側偄曽偑悈幙偺媫寖側曄摦傪偝偣偢偵嵪傒傑偡丅側偍丄崅倫俫丄崅僇儖僔僂儉偱掅俲俫偱偼丄嬻婥拞偺擇巁壔扽慺偑奀悈偵梟偗傗偡偔側傝俲俫偺壓巟偊傪偟傑偡丅乮偄傢偽丄僸僩偑丄擇巁壔扽慺曗媼憰抲偺栶栚傪偟傑偡乯
俀乯墫壔僇儖僔僂儉傪壛偊傞応崌
丂墫壔僇儖僔僂儉扨撈偱壛偊偨応崌丄
丂丂丂丂丂丂丂丂丂丂丂丂丂丂CaCl2亄俀H2O仺Ca乮OH乯2亄俀俫Cl
丂丂丂丂丂丂丂丂丂丂丂丂丂丂Ca乮OH乯2亄俫亄HCO3仺CaCO3伀乮捑揳乯亄俀H2O丂丂偲偄偆斀墳偑偍偒傑偡丅
偡側傢偪丄墫壔僇儖僔僂儉偺扨撈揧壛偼丄俲俫偺掅壓偲丄墫巁晧壸傪傕偨傜偟傑偡丅
丂偙偺偨傔丄墫壔僇儖僔儉傪壛偊傞偲偒偼昁偢丄廳検斾丄俆攞偺廳扽巁僫僩儕僂儉乮廳憘乯傪壛偊傑偡丅偙傟偱丄廳扽巁傪曗媼偟丄僫僩儕僂儉偱丄墫巁傪拞榓偡傞偺偱偡丅
丂丂丂丂丂丂丂丂丂丂丂丂丂丂Na俫CO3亄H2O仺Na亄俷俫-亄俫+亄HCO3-
丂寢壥偲偟偰丄墫壔僫僩儕僂儉丄廳憘暪梡朄偼墫壔僫僩儕僂儉偺帩懕揑晧壸傪傕偨傜偟傑偡丅僫僩儕僂儉傕丄墫慺傕奀悈拞偵懡偔娷傑傟傞尦慺偱偡偺偱丄偡偖偵偼悈憛惗暔偵塭嬁傪梌偊傑偣傫偑丄彊乆偵丄僀僆儞僶儔儞僗傪曵偟偰偄偒傑偡偺偱丄摿偵姺悈検偺彮側偄悈憛偱偼挿婜揑偵偼姪傔傜傟側偄僇儖僔僂儉曗媼朄偱偡丅
俁乯僇儖僔僂儉儕傾僋僞乕傑偨偼僾儗僫儉偐傜曗媼偡傞応崌丅
丂擇巁壔扽慺偑壛偊傜傟偨傝乮僇儖僔僂儉儕傾僋僞乕偺応崌乯丄擇巁壔扽慺偑敪惗偟偨傝偟偰乮僾儗僫儉丄儌僫僐幃悈憛偺応崌乯丄嬊強倫俫偑掅壓偡傞偲偦偙偺扽巁僇儖僔僂儉偼僇儖僔僂儉僀僆儞丗Ca++偲丄廳扽巁僀僆儞丗HCO3-偲側偭偰奀悈拞偵梟偗偩偟偰偒傑偡丅
偙傟偵傛偭偰丄僇儖僔僂儉偺曗廩偲丄俲俫偺忋徃乮廳扽巁僀僆儞偺曗廩乯偑恾傜傟傞巇慻傒偱偡丅崅僇儖僔僂儉偲崅俲俫偑摼傜傟傑偡偑丄傗傗倫俫偑掅偄孹岦偲側傝傑偡丅摿偵僾儗僫儉傗儌僫僐幃偱偼挬偺堦斣倫俫偑掅偄偲偒偼丄倫俫7.8傑偱棊偪傑偡偑丄儈僪儕僀僔側偳偺僴乕僪僐乕儔儖偺惗堢偵偼栤戣偼側偄傛偆偱偡丅
丂寢榑偲偟偰丄
倎乯掅倫俫丄掅俲俫偲掅僇儖僔僂儉偑懚嵼偡傞偲偒偼丄懠偺巁偺嶻惗側偳悈憛僔僗僥儉偵栤戣偑惗偠偰偄傞栿側偺偱丄憗媫側懳張偑昁梫偱偡丅
倐乯僇儖僔儉傪壛偊偰俲俫傪壓偘丄偦傟傪忋偘傛偆偲廳憘傪壛偊丄偙傫偳偼偦傟偱僇儖僔僂儉偑壓偑傝丄傑偨僇儖僔僂儉傪壛偊傞偲偄偆偙偲傪孞傝曉偡偙偲偑偁傝傑偡丅扽巁僇儖僔僂儉偺捑揳偺嶳傪抸偔偙偺乽僋儅偝傫偺僀僗偺媟愗傝乿偵偼傑偭偰偟傑傢側偄傛偆丄奺僇儖僔僂儉偺搳梌朄偵傛傞悈憛摿惈傪傢偒傑偊傞偙偲偑昁梫偱偡丅
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂


 丂丂們倖丏乽倫俫丄俲俫偲僇儖僔僂儉丂曗乿丂
丂丂們倖丏乽倫俫丄俲俫偲僇儖僔僂儉丂曗乿丂