ホームに戻る
酸の分子とイオンの模型アルバム
ミニ授業書<酸の分子とそのイオン>で、酸の分子について新しいイメージが出来たでしょうか? 授業書で出てきた酸の分子の他にも、いろいろな酸の分子があります。
酸の分子の中でも大切な物質と関係の深いものを選んで、その分子模型の写真を示しました。解説と合わせてみて下さい。
|
酸の分子 酸のイオン
|
酸の分子 酸のイオン
|
|

|

|
|
HCl 塩化水素 Cl- 塩素イオン
(水溶液が塩酸) (塩化物イオン)
白:水素原子、 肌色:塩素原子
|
H2SO4 硫酸 SO42- 硫酸イオン
赤:酸素原子、 黄:硫黄原子
|
|

|

|
|
H2S 硫化水素 S2- 硫黄イオン
(硫化物イオン)
白:水素原子、 黄:硫黄原子
|
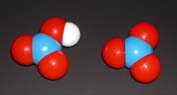
H3PO4 リン酸 PO43-
リン酸イオン
茶:リン原子
|
|

|
|
|
H2O 水 OH- 水酸化物イオン
(酸化水素) 赤:酸素原子
|
HNO3 硝酸
NO3-
硝酸イオン
青:窒素原子
|
|

|

|
|
H3O+ H2O 水
オキソニウムイオン
|
H2CO3 炭酸
CO32-
炭酸イオン
黒:炭素原子
|
|

|

|
|
NH4+ NH3 アンモニア
アンモニウムイオン 青:窒素原子
|
CH3COOH 酢酸 CH3COO- 酢酸イオン
黒:炭素原子
|
写真の分子模型は、由良製作所製のプラスチック分子模型を使用しています。
仮説社(tel:03-3204-1779)で購入できます。
解 説
酸の分子には、分子から離れやすい水素原子(H)があります。酸の分子(HA)が水などの他の分子(B)に出会うと、この水素原子が相手分子に移動します。
水素原子は移動するときに、電子を酸の分子(HA)に残していくので、酸の分子はマイナスの電気が多くなります。このマイナスの電気を帯びた状態を、もとの酸の分子(HA)と区別して酸のイオン(A-)といいます。
HA ⇔ A-+
H+・・・(1)
分子(B)は、酸の分子(HA)から電子不足の水素原子(H+)を受け取ると、水素原子が1個増えプラスの電気を帯びます。この状態の分子(BH+)はプラスのイオンです。
B
+
H+ ⇔ BH+・・・(2)
(1)と(2)の反応は、同時に起きるので、2つを合わせると次のように表せます。
HA +
B ⇔ A-+
BH+
上に示した分子の中には、水のように普通は酸といわないものも含まれていますが、他の分子に移動する水素原子を持っているので、酸の仲間に入れることが出来ます。
また、オキソニウムイオン(H3O+)やアンモニウムイオン(NH4+)のように、酸の性質をもったイオンもあります。
H+が他の分子に移動すると、イオンが分子になります。
ホームに戻る









